Open time:..
The Last Update Time:..
朱志伟,博士,教授,国家级青年人才项目入选者
2008年毕业于华东理工大学理工优秀生部生物工程专业获工学学士学位;2014年毕业于中科院大连化学物理研究所获生物化工博士学位;2014-2019年,在瑞典查尔姆斯理工大学从事博士后研究;2020年1月,加入大连理工大学生物工程学学院任教授,组建代谢工程与合成生物技术课题组;2020年2月-4月,在德国法兰克福大学从事访问研究。
主要研究方向为微生物合成代谢工程,即通过合成生物学技术(高级基因工程手段)操纵微生物代谢,提升脂质、多元醇等绿色生物化学品的合成效率,以达到产业应用水平;同时组合多种组学分析、生物信息学、计算设计和蛋白结构分析等,实现多维度、跨尺度微生物设计和改造,构建智能化的微生物细胞工厂。
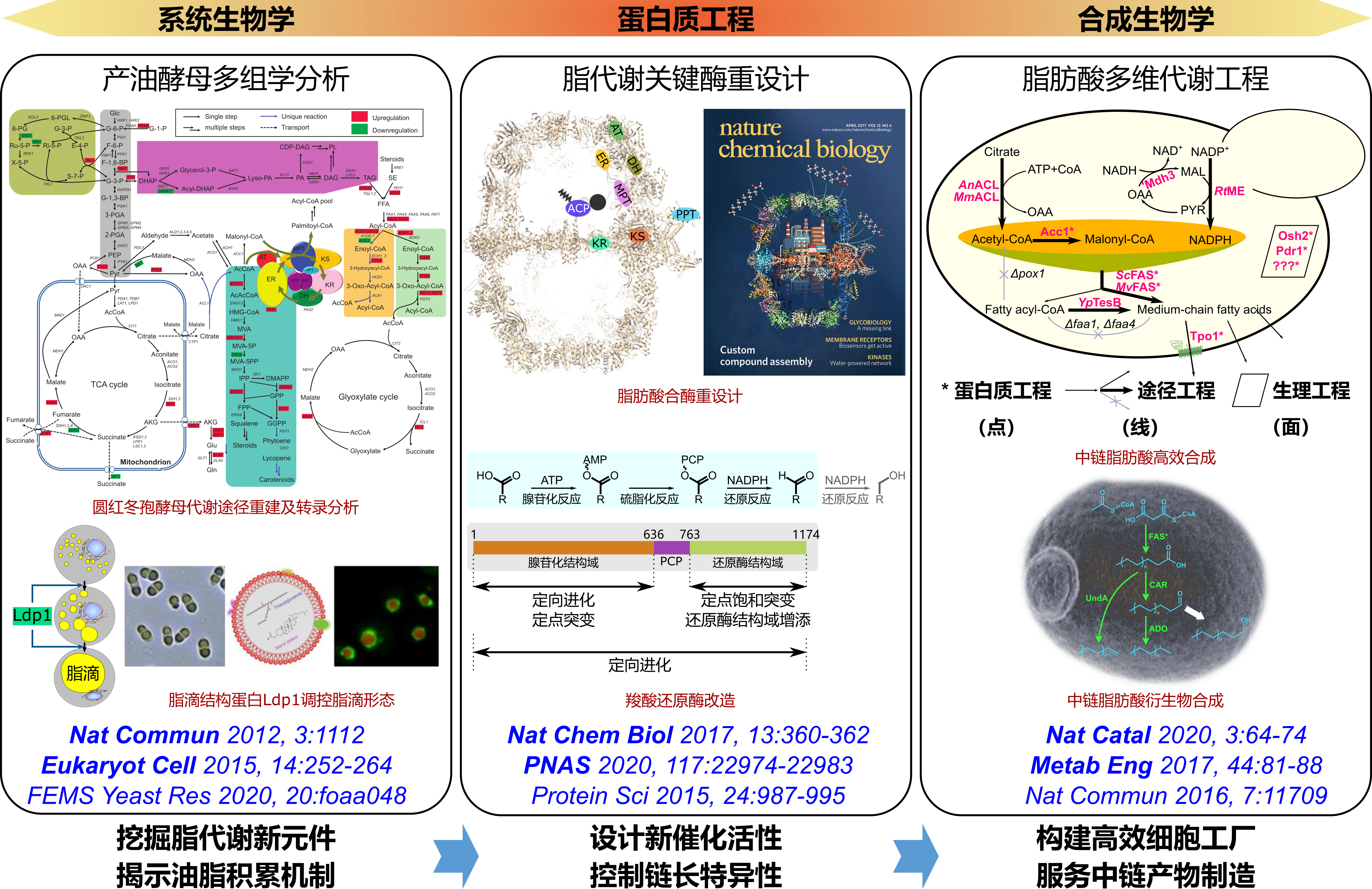
已在脂质代谢相关的燃料和化学品生物制造领域,如产油酵母多组学分析、脂代谢关键酶重设计、脂肪酸多维代谢工程等方向取得重要进展。
(1)率先开展产油酵母多组学分析,精确注释了圆红冬孢酵母基因组,重建其油脂合成代谢网络,发现含双酰基载体蛋白结构域脂肪酸合酶、酵母脂滴蛋白等决定产油表型的关键元件,从系统生物学角度揭示了氮源限制导致油脂积累的分子机制。
(2)对前述新颖脂肪酸合酶进行了详细的酶学和结构表征,首次重设计构建出杂合的真菌I型脂肪酸合酶,扩展其产物谱,打破了该类复合物不可改造的固有认识,开辟了油脂化学品合成新路线,论文被Nat Chem Biol杂志选作封面,且同期配发专文推荐,受到30多家媒体关注和报道,相关专利转让给法国石油巨头道达尔公司,并受邀在酵母脂质代谢顶级会议(YLC2017)做分会场报告。
(3)提出多维代谢工程策略,在蛋白/酶工程改造层次、代谢途径优化层次和细胞耐受性改善层次,多维度改造酵母合成并分泌大量中链脂肪酸,使产量提高250倍以上,发酵产量达到3 g/L,为真核微生物合成的最高水平,相关成果发表在Nat Catal杂志,被生物工程领域权威综述期刊Trends Biotechnol杂志推荐报道。
(4)已发表论文22篇,其中在Nat Chem Biol、Nat Catal、Nat Commun、PNAS等期刊发表一作论文多篇;获国内专利授权3项,国际PCT专利授权1项;荣获辽宁省自然科学二等奖(排名第二)、大连市技术发明一等奖(排名第四)、15届国际生物技术大会(IBS2012)最佳墙报奖等奖项;在国际可再生资源与生物炼制大会(RRB13)等国际学术会议做口头报告或墙报展示10余次,担任Engineering in Life Sciences杂志编委,Metab Eng、Biotechnol Bioeng、ACS Synth Biol、Appl Environ Microbiol等期刊审稿人。入选国家级青年人才计划、校“星海青千”、大连市“高端人才”。
近期主持与参与的科研项目如下:
1. 国家自然科学基金--优秀青年基金项目(海外),主持
2. 国家重点研发计划课题(项目编号:2022YFA0911802):高效基因组编辑与遗传体系建立及途径组装与整合改造,2022.11-2027.10。所属项目:工业菌株重编程优化及应用,所属专项:合成生物学,参与
3. 国家重点研发计划课题(项目编号:2021YFC2103702):油脂生物合成及航空燃料制备关键生物催化剂结构解析、优化及应用,2021.12-2024.11。所属项目:先进航空燃料生物制造技术,所属专项:绿色生物制造,主持
4. 国家自然科学基金--面上基金(项目编号:22177018):基于酰基载体蛋白定量调控机制重设计真菌I型脂肪酸合酶,2022.01-2025.12,主持
5. 企业横向项目,2022.07-2025.07,主持
6. 中央高校基本科研业务费引进人才科研专题(项目编号:DUT20RC(3)044):中链脂肪酸及其衍生物微生物制造,2020.08-2022.12,主持
代谢工程与合成生物技术研究课题组,拥有实验办公用房约120平方,配备优良的学习、办公与实验环境,课题组购置实时微生物生长分析系统、酵母孢子解剖显微镜、气相色谱仪、低温超高压细胞破碎仪、恒温振荡培养箱、洗瓶机、低温高速离心机、高压灭菌锅、超低温冰箱、生物样品均质机、凝胶成像系统、电穿孔仪、梯度PCR仪、分光光度计等仪器50余台(套),满足分子生物学操作、微生物培养与发酵、产物提取与分析所需之实验条件。课题组现有教授1名,博士研究生4名,硕士研究生8名。已指导本科毕业生7名,6人进入本校及复旦大学、中科院先进技术研究院合成生物学研究所、北京师范大学、江南大学深造。共同指导本科生团队DUT_China获得2020年iGEM大赛金奖、”互联网+“大赛辽宁省银奖等。
课题组现有成员
| 姓名 | 入学时间 | 攻读学位 | 专业 | 联系方式 | 毕业去向 |
|---|---|---|---|---|---|
| 张乔馨 | 2020.09 | 硕博连读研究生 | 化学工程 | xxx@xxx.xx.xx | - |
| 谭亚娣 | 2020.09 | 硕博连读研究生 | 生物工程 | xxx@xxx.xx.xx | - |
| 冯彩 | 2023.09 | 博士研究生 | 生物工程 | xxx@xxx.xx.xx | - |
| 姜逸 | 2023.09 | 博士研究生 | 化学工程 | xxx@xxx.xx.xx | |
| 李明君 | 2021.09 | 硕士研究生 | 生物与医药 | xxx@xxx.xx.xx | - |
| 王欣凯 | 2021.09 | 硕士研究生 | 生物学 | xxx@xxx.xx.xx | - |
| 曾威阳 | 2022.09 | 硕士研究生 | 生物工程 | xxx@xxx.xx.xx | - |
| 孙卓 | 2022.09 | 硕士研究生 | 生物工程 | xxx@xxx.xx.xx | - |
| 赵硕 | 2022.09 | 硕士研究生 | 生物技术与工程 | xxx@xxx.xx.xx | - |
| 李婧琦 | 2022.09 | 硕士研究生 | 生物技术与工程 | xxx@xxx.xx.xx | - |
| 杨静 | 2023.09 | 硕士研究生 | 生物学 | xxx@xxx.xx.xx | - |
| 胡孟凡 | 2023.09 | 硕士研究生 | 生物学 | xxx@xxx.xx.xx | - |
| 高荣君 | 2023.09 | 硕士研究生 | 生物学 | xxx@xxx.xx.xx | - |
| 王文亮 | 2020.09 | 硕士 | 生物与医药 | xxx@xxx.xx.xx | 科研助理 |
本课题组热情欢迎各类人才加入,欢迎来信咨询,Email:zwzhu@dlut.edu.cn
1. 准聘教授/副教授,助理教授:欢迎海内外青年才俊加入,除国家、省、市、学校、学院提供的支持外,课题组也将竭力支持新加入老师的发展。
2. 助理研究员(博士后)招聘(长期有效,欢迎来信咨询):本课题组正在承担多项国家与企业委托项目,因研究需要,诚聘具有微生物学、分子生物学、代谢工程与合成生物学、生物信息学研究背景的助理研究员,3年合同,基本年薪30万,可申请大连市青年才俊30万安家费补贴(分3年发放,18/6/6万),期满优秀者聘为副教授。应聘要求及待遇请查询学校人事处网站或来信咨询。
3. 科研助理岗位A(可兼职):本科学历,生物、化学等相关专业,主要职责包括(1)协助实验室管理,如试剂耗材采购与报销、仪器设备管理与维护、实验室安全等;(2)负责项目资料收集与整理;(3)参与研究开发,如微生物菌株构建与性能评价;(4)课题组长交办的其他事务。岗位待遇按照《大连理工大学科研项目自聘人员管理办法(试行)》 执行。
4. 科研助理岗位B:硕士及以上学历,微生物学、分子生物学、代谢工程、合成生物学、生物信息学等相关专业,主要职责为代谢工程与合成生物学技术开发,包括质粒构建、途径组装、遗传转化、微生物培养发酵,产物分析检测等研究内容。岗位待遇按照《大连理工大学科研项目自聘人员管理办法(试行)》 执行。
5. 科研助理岗位C:针对应届毕业生,学习积极努力,有意向留组攻读硕士或博士学位,且符合项目需要,可以科研助理形式聘任留组工作到研究生入学。岗位待遇参考同期硕士和博士助研津贴,并提供租房补贴。
6. 博士研究生招生:课题组每年有1-2个博士生研究生招生名额,为申请考核制,每年10-12月准备申请材料,有意申请博士的同学欢迎邮件联系。
7. 硕士研究生招生:课题组每年有4个硕士研究生招生名额(学术型和专业型各2名),欢迎邮件联系。
1. Zhiwei Zhu, Yongjin J. Zhou, Anastasia Krivoruchko, Martin Grininger, Zongbao K. Zhao* & Jens Nielsen*. (2017). Expanding the product portfolio of fungal type I fatty acid synthases. Nature Chemical Biology, 13(4), 360-362. doi:10.1038/nchembio.2301
Cover story, News and Views by Timm Maier. (2017). Fatty acid synthases: Re-engineering biofactories. Nature Chemical Biology, 13(4), 344-345. doi:10.1038/nchembio.2338
2. Zhiwei Zhu#, Yating Hu#, Paulo G. Teixeira, Rui Pereira, Yun Chen, Verena Siewers & Jens Nielsen*. (2020). Multidimensional engineering of Saccharomyces cerevisiae for efficient synthesis of medium-chain fatty acids. Nature Catalysis, 3(1), 64-74. doi:10.1038/s41929-019-0409-1
Highlight by Jianhui Liu & Jin Hou. (2020). Multidimensional Metabolic Engineering for Constructing Efficient Cell Factories. Trends in Biotechnology, 38(5), 468-469. doi:10.1016/j.tibtech.2020.02.011
3. Zhiwei Zhu, Sufang Zhang, Hongwei Liu, Hongwei Shen, Xinping Lin, Fan Yang, Yongjin J. Zhou, Guojie Jin, Mingliang Ye, Hanfa Zou* & Zongbao K. Zhao*. (2012). A multi-omic map of the lipid-producing yeast Rhodosporidium toruloides. Nature Communications, 3, 1112. doi:10.1038/ncomms2112
4. Yating Hu#, Zhiwei Zhu#, David Gradischnig, Margit Winkler, Jens Nielsen* & Verena Siewers. (2020). Engineering carboxylic acid reductase for selective synthesis of medium-chain fatty alcohols in yeast. Proceedings of the National Academy of Sciences, 202010521. doi:10.1073/pnas.2010521117
5. Zhiwei Zhu, Yongjin J. Zhou, Min-Kyoung Kang, Anastasia Krivoruchko, Nicolaas A. Buijs & Jens Nielsen*. (2017). Enabling the synthesis of medium chain alkanes and 1-alkenes in yeast. Metabolic Engineering, 44, 81-88. doi:10.1016/j.ymben.2017.09.007
2023
24. Guimin Liu#, Cai Feng#, Zhiwei Zhu, Yaqin Sun, and Zhilong Xiu. (2023). Fed-Batch Self-Regulated Fermentation of Glucose to Co-Produce Glycerol and 1,3-Propanediol by Recombinant Escherichia Coli. Synthetic Biology and Engineering 1(1), 1-10. 10.35534/sbe.2023.10008.
2021
23. 朱志伟*, 谭亚娣, 张乔馨 & 薛闯. (2021). 中链化学品微生物制造. 微生物学杂志, (5), 1-13. doi:10.3969/j.issn.1005-7021.2021.05.001
2020
22. Yating Hu#, Zhiwei Zhu#, David Gradischnig, Margit Winkler, Jens Nielsen* & Verena Siewers. (2020). Engineering carboxylic acid reductase for selective synthesis of medium-chain fatty alcohols in yeast. Proceedings of the National Academy of Sciences, 202010521. doi:10.1073/pnas.2010521117
21. Renhui Zhou#, Zhiwei Zhu#, Sufang Zhang* & Zongbao K. Zhao. (2020). The complete mitochondrial genome of the lipid-producing yeast Rhodotorula toruloides. FEMS Yeast Research. doi:10.1093/femsyr/foaa048
20. Zhiwei Zhu#, Yating Hu#, Paulo G. Teixeira, Rui Pereira, Yun Chen, Verena Siewers & Jens Nielsen*. (2020). Multidimensional engineering of Saccharomyces cerevisiae for efficient synthesis of medium-chain fatty acids. Nature Catalysis, 3(1), 64-74. doi:10.1038/s41929-019-0409-1
2019
19. Yating Hu, Zhiwei Zhu, Jens Nielsen* & Verena Siewers. (2019). Engineering Saccharomyces cerevisiae cells for production of fatty acid derived biofuels and chemicals. Open Biology, 9(5), 190049. doi:10.1098/rsob.190049
2018
18. Yongjin J. Zhou*, Yating Hu, Zhiwei Zhu, Verena Siewers & Jens Nielsen*. (2018). Engineering 1-Alkene Biosynthesis and Secretion by Dynamic Regulation in Yeast. ACS Synthetic Biology, 7(2), 584-590. doi:10.1021/acssynbio.7b00338
17. Yanan Wang, Sufang Zhang*, Zhiwei Zhu, Hongwei Shen, Xinping Lin, Xiang Jin, Xiang Jiao & Zongbao K. Zhao*. (2018). Systems analysis of phosphate-limitation-induced lipid accumulation by oleaginous yeasts Rhodosporidium toruloides. Biotechnology for Biofuels, 11, 148. doi:10.1186/s13068-018-1134-8
16. Yating Hu, Zhiwei Zhu, Jens Nielsen & Verena Siewers*. (2018). Heterologous transporter expression for improved fatty alcohol secretion in yeast. Metabolic Engineering, 45, 51-58. doi:10.1016/j.ymben.2017.11.008
2017
15. Zhiwei Zhu, Yongjin J. Zhou, Anastasia Krivoruchko, Martin Grininger, Zongbao K. Zhao* & Jens Nielsen*. (2017). Expanding the product portfolio of fungal type I fatty acid synthases. Nature Chemical Biology, 13(4), 360-362. doi:10.1038/nchembio.2301
14. Zhiwei Zhu, Yongjin J. Zhou, Min-Kyoung Kang, Anastasia Krivoruchko, Nicolaas A. Buijs & Jens Nielsen*. (2017). Enabling the synthesis of medium chain alkanes and 1-alkenes in yeast. Metabolic Engineering, 44, 81-88. doi:10.1016/j.ymben.2017.09.007
2016
13. Yongjin J. Zhou, Nicolaas A. Buijs, Zhiwei Zhu, Jiufu Qin, Verena Siewers & Jens Nielsen*. (2016). Production of fatty acid-derived oleochemicals and biofuels by synthetic yeast cell factories. Nature Communications, 7, 11709. doi:10.1038/ncomms11709
12. Yongjin J. Zhou* #, Nicolaas A. Buijs#, Zhiwei Zhu, Diego Orol Gómez, Akarin Boonsombuti, Verena Siewers & Jens Nielsen*. (2016). Harnessing Yeast Peroxisomes for Biosynthesis of Fatty-Acid-Derived Biofuels and Chemicals with Relieved Side-Pathway Competition. Journal of the American Chemical Society, 138(47), 15368-15377. doi:10.1021/jacs.6b07394
2015
11. Zhiwei Zhu#, Yunfeng Ding#, Zhiwei Gong, Li Yang, Sufang Zhang, Congyan Zhang, Xinping Lin, Hongwei Shen, Hanfa Zou, Zhensheng Xie, Fuquan Yang, Xudong Zhao, Pingsheng Liu* & Zongbao K. Zhao*. (2015). Dynamics of the Lipid Droplet Proteome of the Oleaginous Yeast Rhodosporidium toruloides. Eukaryotic Cell, 14(3), 252-264. doi:10.1128/ec.00141-14
10. Manuel Fischer, Daniel Rhinow, Zhiwei Zhu, Deryck J. Mills, Zongbao K. Zhao, Janet Vonck & Martin Grininger*. (2015). Cryo-EM structure of fatty acid synthase (FAS) from Rhodosporidium toruloides provides insights into the evolutionary development of fungal FAS. Protein Science, 24(6), 987–995. doi:10.1002/pro.2678
2014
9. 朱志伟, 张素芳, 林心萍, 刘武军 & 赵宗保*. (2014). 圆红冬孢酵母新颖脂肪酸合酶的重组表达、纯化与活性检测. 生物工程学报, 30(9), 1414–1423. doi:10.13345/j.cjb.130626
8. 刘玉雪, 张祎昕, 王磊, 林心萍, 朱志伟 & 赵宗保*. (2014). 重组酿酒酵母催化二氢大豆苷元生产雌马酚. 中国生物工程杂志, 34(4), 41-45. doi:10.13523/j.cb.20140407
7. Xinping Lin, Yanan Wang, Sufang Zhang, Zhiwei Zhu, Yongjin J. Zhou, Fan Yang, Wenyi Sun, Xueying Wang & Zongbao K. Zhao*. (2014). Functional integration of multiple genes into the genome of the oleaginous yeast Rhodosporidium toruloides. FEMS Yeast Research, 14(4), 547-555. doi:10.1111/1567-1364.12140
2013
6. Yongjin J. Zhou, Wei Yang, Lei Wang, Zhiwei Zhu, Sufang Zhang & Zongbao K. Zhao*. (2013). Engineering NAD+ availability for Escherichia coli whole-cell biocatalysis: a case study for dihydroxyacetone production. Microbial Cell Factories, 12(1), 103. doi:10.1186/1475-2859-12-103
5. 蔡媛, 郭娟, 周雍进, 朱志伟, 吴文燕, 黄璐琦, 陈敏*, & 赵宗保. (2013). 转化次丹参酮二烯酿酒酵母全细胞催化体系的构建. 药学学报, 48(10), 1618-1623.
2012
4. Zhiwei Zhu, Sufang Zhang, Hongwei Liu, Hongwei Shen, Xinping Lin, Fan Yang, Yongjin J. Zhou, Guojie Jin, Mingliang Ye, Hanfa Zou* & Zongbao K. Zhao*. (2012). A multi-omic map of the lipid-producing yeast Rhodosporidium toruloides. Nature Communications, 3, 1112. doi:10.1038/ncomms2112
3. Yongjin J. Zhou#, Wei Gao#, Qixian Rong, Guojie Jin, Huiying Chu, Wujun Liu, Wei Yang, Zhiwei Zhu, Guohui Li, Guofeng Zhu, Luqi Huang*, & Zongbao K. Zhao*. (2012). Modular pathway engineering of diterpenoid synthases and the mevalonic acid pathway for miltiradiene production. Journal of the American Chemical Society, 134(6), 3234–3241. doi:10.1007/s00253-011-3820-3
2. Fan Yang, Sufang Zhang, Yongjin J. Zhou, Zhiwei Zhu, Xinping Lin, & Zongbao K. Zhao*. (2012). Characterization of the mitochondrial NAD+-dependent isocitrate dehydrogenase of the oleaginous yeast Rhodosporidium toruloides. Applied Microbiology and Biotechnology, 94(4), 1095-1105. doi:10.1007/s00253-011-3820-3
1. Xinping Lin, Fan Yang, Yongjin Zhou, Zhiwei Zhu, Guojie Jin, Sufang Zhang*, & Zongbao K. Zhao. (2012). Highly-efficient colony PCR method for red yeasts and its application to identify mutations within two leucine auxotroph mutants. Yeast, 29(11), 467-474. doi:10.1002/yea.2926
中国科学院大学 生物化工 Doctoral Degree
华东理工大学 生物工程 Bachelor's Degree
湖南省双峰一中 \
大连理工大学生物工程学院 教授
瑞典查尔姆斯理工大学 博士后